Weltweiter Kundendienst
Unique Device Identification (UDI)
Am 24 September 2013 veröffentlichte die United States Food and Drug Administration (FDA) eine finale Regelung mit der Anforderung, dass die meisten Medizinprodukte, die in den Vereinigten Staaten vertrieben werden, einen Unique Device Identifier (UDI) tragen müssen. Das UDI-System ermöglicht die Identifizierung und Nachverfolgbarkeit von Medizinprodukten im Vertrieb und Gebrauch. Die Regelung macht es erforderlich, dass Produktinformationen zu den Geräten bei der Global Unique Device Identification Database (GUDID) der FDA eingereicht werden.
Außerdem enthält die Regelung die Verpflichtung zur Verwendung eines neuen, standardisierten Datumsformats bei allen Kennzeichnungen von Medizinprodukten.
Masimo hat seine Kennzeichnungspraxis so angepasst, dass sie die UDI-Regelung und die GS1-Standards erfüllt.
Wenn Sie Fragen haben, die nicht von diesen FAQs abgedeckt werden, wenden Sie sich bitte an den Kundendienst:
USA: customerorders@masimo.com
Außerhalb der USA: emeasales@masimo.com
1. Was ist ein UDI?
Ein Unique Device Identifier (UDI) besteht aus einer Reihe von numerischen oder alphanumerischen Zeichen, die einem weltweit geltenden Kodierungsstandard folgt und ein Gerät an der Stelle des Vertriebs und Gebrauchs hinreichend identifizierbar macht. Ein UDI besteht aus:
- Eine Gerätekennung, die GTIN (Global Trade Item Number): ein fester Pflichtbestandteil des UDIs, der die spezifische Version bzw. das Modell des Geräts und die kennzeichnende Stelle angibt, sowie
- Eine Produktionskennung: ein nur unter bestimmten Umständen vorhandener, variabler Bestandteil des UDIs, der für eine oder mehrere der folgenden Informationen steht, wenn er Teil der Gerätekennzeichnung ist:
- Das Fertigungslos oder die Charge, zu der das Gerät gehört
- Die Seriennummer des spezifischen Geräts
- Das Verfallsdatum des spezifischen Geräts und/oder
- Das Datum, an dem das spezifische Gerät hergestellt wurde
Masimos akkreditierte Stelle zur Zuweisung von Strichcodes und Strichcodestrukturen ist GS1 .
Bitte beachten Sie, dass Produkte, die NICHT als Medizinprodukte eingestuft sind, keinen Strichcode tragen müssen.
2. Wer muss die UDI-Regelungen einhalten?
Alle Unternehmen, die Medizinprodukte herstellen, müssen die UDI-Regelungen einhalten.
3. Welche Frist gilt für die Umsetzung der UDI-Regelungen?
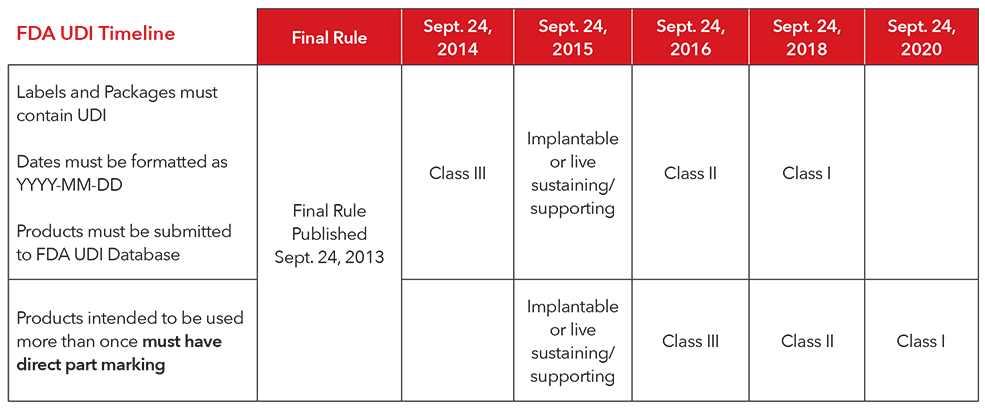
4. Wie plant Masimo, die UDI-Regelungen zu erfüllen?
Masimo vertreibt Produkte der Klasse II und eine geringe Zahl von Produkten der Klasse I. Masimo hat seine Kennzeichnungspraxis so angepasst, dass sie die UDI-Regelung und GS1-Standards erfüllt.
Bitte beachten Sie, dass Produkte, die NICHT als Medizinprodukte eingestuft sind, keinen Strichcode tragen müssen.
5. Wie wird die neue UDI- und direkte Teilekennzeichnung aussehen?
Im Folgenden finden Sie Beispiele für:
- Etiketten auf Schachteln für Sensoren mit der vorigen Version und der aktualisierten UDI-Kennzeichnung
- Ein Sensor mit direkter Teilekennzeichnung
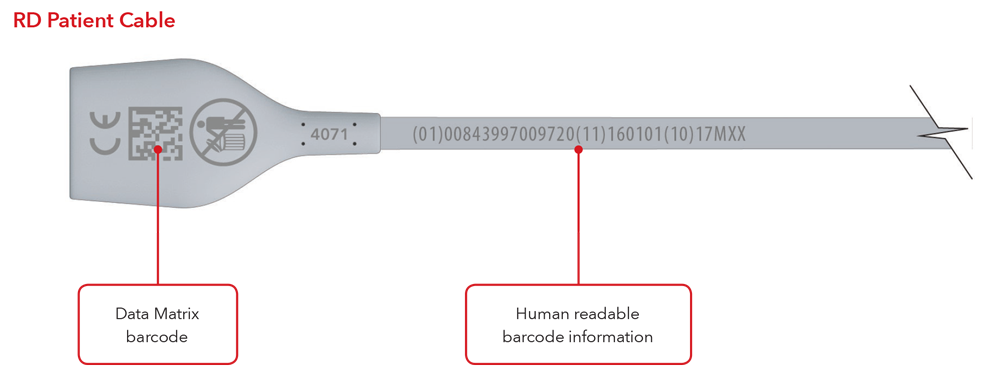
- Ein Kabel mit direkter Teilekennzeichnung
Bitte beachten: Je nach Produkttyp enthält das Etikett eins von zwei Daten. Bei Produkten mit einem Verfallsdatum ist dieses im Format JJJJ-MM-TT unter dem Symbol des Verfallsdatums angegeben und außerdem im Format JJMMTT mit vorangestellter Produktionskennung (17) als Teil des GS1- und 2D-Strichcodes kodiert. Bei Produkten ohne Verfallsdatum ist das Herstellungsdatum im Format JJJJ-MM-TT direkt neben dem Symbol für das Herstellungsdatum angegeben und außerdem im Format JJMMTT mit vorangestellter Produktionskennung (11) als Teil des GS1- und 2D-Strichcodes kodiert.
Beispiele für Etiketten auf Sensorschachteln
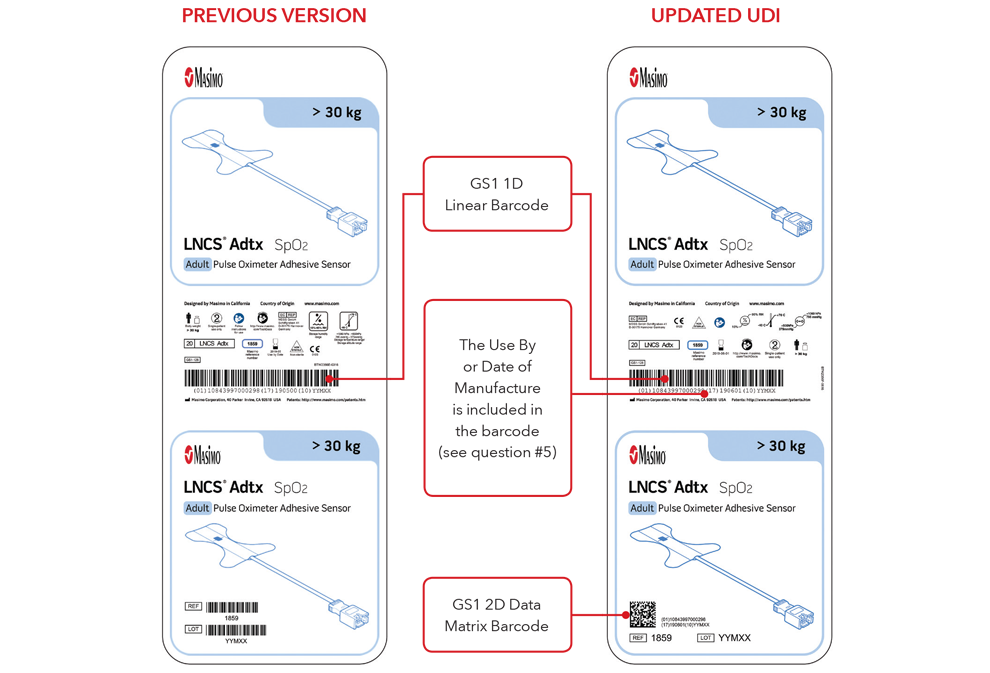
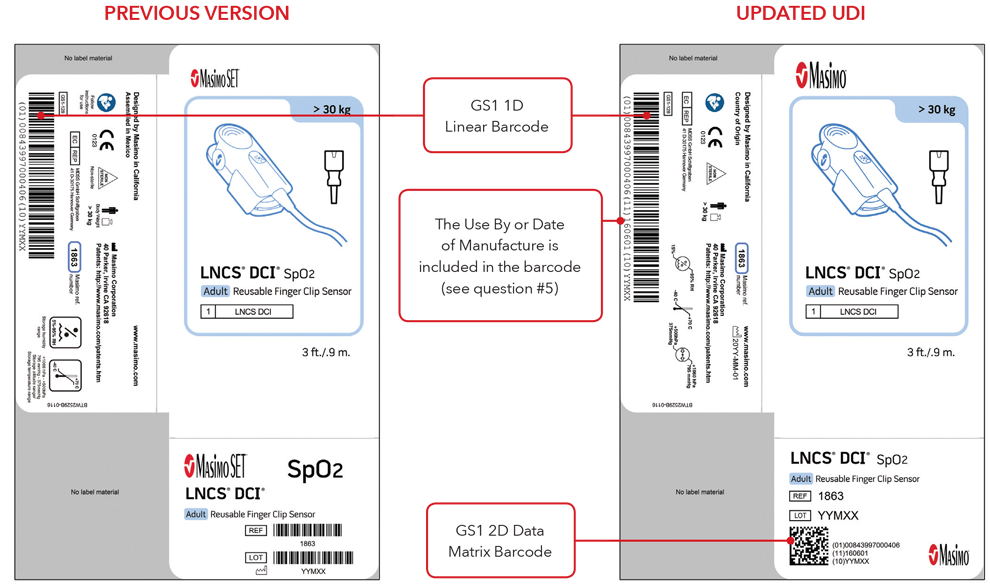
Beispiele für Sensoren und Kabel mit direkter Teilekennzeichnung
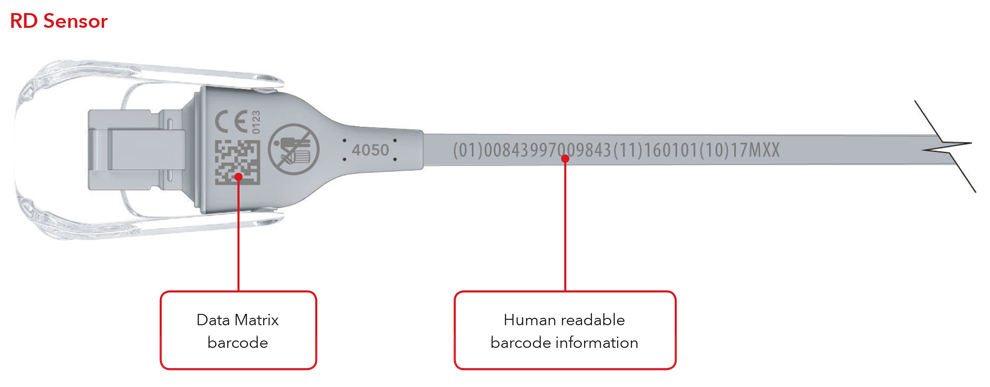
6. Was ist eine Global Trade Item Number (GTIN)?
Eine GTIN ist ein weltweit eindeutige GS1-Identifikationsnummer, die zur Identifizierung eines Handelsguts dient. GTINs werden vom Inhaber der Marke des Produkts (der kennzeichnenden Stelle) zugewiesen und zur Identifizierung von Produkten auf dem Weg zum Verbraucher, etwa einem Krankenhaus, entlang der globalen Lieferkette eingesetzt. Wenn Sie das GS1-System mit GTINs momentan nicht zur Verwaltung Ihrer Produkte nutzen, müssen Sie die GTINs für die Produkte anfordern, die Sie einkaufen.
Um weitere Informationen über GTINs zu erhalten, wenden Sie sich an GS1 unter: https://www.gs1us.org/what-we-do/standards.
7. Wie erhalte ich GTINs für Produkte?
Per E-Mail an den Masimo-Kundendienst:
USA: customerorders@masimo.com
Außerhalb der USA: emeasales@masimo.com
Bitte geben Sie in der E-Mail Ihre Kunden-ID und die Teilenummern der Produkte an.
8. Momentan gebe ich die LOT- und/oder REF-Strichcodes von Masimo auf dem Etikett ein oder scanne sie. Ist zu erwarten, dass ich dieses Verfahren nicht mehr störungsfrei anwenden kann?
Ja. Die LOT- und REF-Strichcodes werden nicht mehr auf dem Etikett erscheinen, sondern durch Text ersetzt. Ein Scannen ist nicht mehr möglich. Um die LOT-Informationen zu erhalten, müssen Sie entweder den GS1-Strichcode scannen oder die Informationen neben dem LOT-Symbol auf dem Etikett ablesen. Die REF-Informationen lassen sich durch die jeweilige GTIN bestimmen. Weitere Informationen zu GTINs finden Sie oben bei Frage 6.
9. Werden sich die Masimo-Produktnummern ändern, wenn die UDI-Kennzeichnung eingeführt wird?
Nein, die Masimo-Produktnummern bleiben gleich.
10. Wie lautet das neue standardisierte Datumsformat und wann tritt es in Kraft?
Im Rahmen der UDI-Regelung wird bei Gerätekennzeichnungen das standardisierte Datumsformat JJJJ-MM-TT verwendet. Das neue Format wird spätestens dann für Daten auf Etiketten verwendet, wenn das Geräteetikett verpflichtend einen UDI tragen muss. Weitere Informationen zum zeitlichen Ablauf der Umsetzung finden Sie oben bei Frage 3.
11. Wird Masimo Produktinformationen online zur Verfügung stellen?
Die GUDID ist eine öffentlich zugängliche, durchsuchbare Datenbank, die den Teil zur Geräteinformation (DI) des UDIs für jedes Medizinprodukt sowie weitere verpflichtend anzugebende Produktinformationen enthält. Alle Unternehmen, die Medizinprodukte herstellen, müssen bei der GUDID DI-Informationen einreichen. Masimo hat mit der Dateneingabe in die GUDID begonnen und stellt sicher, dass der Datenbank alle Produkte gemäß den UDI-Umsetzungsfristen oder früher hinzugefügt werden.
12. Was ist mit Bestandsinventar? Müssen die Hersteller solche Produkte umetikettieren?
Nein, es gibt zwei Ausnahmen für Bestandinventar:
- Geräte, die sich vor dem jeweils geltenden Datum des Inkrafttretens im Umlauf befanden, müssen die finale Regelung nicht erfüllen.
- Geräte, die vor dem jeweils geltenden Datum des Inkrafttretens hergestellt und gekennzeichnet wurden, sind ebenfalls von der Pflicht ausgenommen. Diese Ausnahmen gelten allerdings nur für einen Zeitraum von 3 Jahren nach dem jeweils geltenden Datum des Inkrafttretens.
13. Müssen alle Geräte direkt mit dem UDI gekennzeichnet werden?
Nein. Die Regelung erfordert nur bei wiederverwendbaren Medizinprodukten, die vor dem erneuten Gebrauch wiederaufbereitet werden müssen (hoher Reinigungsstandard oder Sterilisation), eine direkte Kennzeichnung.
Weitere Informationen zum zeitlichen Ablauf der Umsetzung der direkten Kennzeichnung finden Sie oben bei Frage 3.
Weitere Informationen über das UDI-System erhalten Sie unter „Unique Device Identification (UDI)“ auf der FDA-Website:
http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/UniqueDeviceIdentification/
Sollten Sie weitere Fragen zur Einhaltung der UDI-Regelungen durch Masimo haben, wenden Sie sich bitte an den Masimo-Kundendienst unter:
USA: customerorders@masimo.com
Außerhalb der USA: emeasales@masimo.com
PLCO-008044/ PLMM-12789A-0326 EN- PLMM-10045D