Unique Device Identification (UDI, einzigartige Produktkennzeichnung)
Globale Dienste
Home / UDI-Kennzeichnung
UDI-Kennzeichnung
Am 24. September 2013 hat die FDA (United States Food and Drug Administration) endgültig beschlossen, dass die meisten in den USA vertriebenen medizinischen Geräte sog. Unique Device Identifiers (UDIs, einzigartige Produktkennzeichnungen) tragen müssen. Das UDI-System vereinfacht Identifikation, Rückverfolgbarkeit und Verfolgung von medizinischen Geräten während des Vertriebs und im Einsatz. Der Beschluss sieht vor, dass die Produktinformationen zu den Geräten der Global Unique Device Identification Database (GUDID) der FDA zu melden sind.
Zudem sieht der Beschluss vor, dass ein neues, standardisiertes Datumsformat auf allen Kennzeichnungen von medizinischen Geräten zu verwenden ist.
Masimo hat die Kennzeichnung entsprechend den Anforderungen der UDI-Vorschrift und GS1-Standards aktualisiert.
Haben Sie noch Fragen über diese FAQs hinaus, wenden Sie sich bitte an den Kundenservice:
USA: customerorders@masimo.com
Außerhalb der USA: emeasales@masimo.com
Häufig gestellte Fragen
Häufig gestellte Fragen
1. Was bedeutet UDI?
Ein Unique Device Identifier (UDI) ist eine Reihe von alphanumerischen Zeichen auf Basis einer globalen Codierungsnorm, die ein Gerät am Vertriebsstandort und am Verwendungsstandort hinreichend identifiziert. Ein UDI besteht aus:
- Einer Geräte-Identifikationsnummer, der GTIN (Global Trade Item Number): ein obligatorischer, festgelegter Teil eines UDI, der die genaue Version oder das Gerätemodell identifiziert, ebenso wie die kennzeichnende Stelle; und
- Einer Produktions-Identifikationsnummer: ein von einigen Faktoren abhängiger, veränderlicher Teil eines UDI, der eine oder mehr der folgenden Informationen identifiziert, sofern auf der Gerätekennzeichnung aufgeführt:
- Die Produktionscharge, in der ein Gerät hergestellt worden ist;
- Die Seriennummer eines bestimmten Geräts;
- Das Verfallsdatum eines bestimmten Geräts; und/oder
- Das Datum, an dem ein bestimmtes Gerät hergestellt worden ist.
Masimo arbeitet für das Zuordnen von Barcodes und Barcode-Strukturen mit GS1 als akkreditierter Stelle zusammen.
Bitte beachten Sie, dass alle Produkte, die NICHT als medizinisches Gerät klassifiziert sind, keinen Barcode tragen müssen.
2. Wer muss sich an die UDI-Verordnungen halten?
Alle Unternehmen, die medizinische Geräte herstellen, müssen sich an die UDI-Verordungen halten.
3. Innerhalb welchen Zeitrahmens müssen die UDI-Verordungen umgesetzt werden?
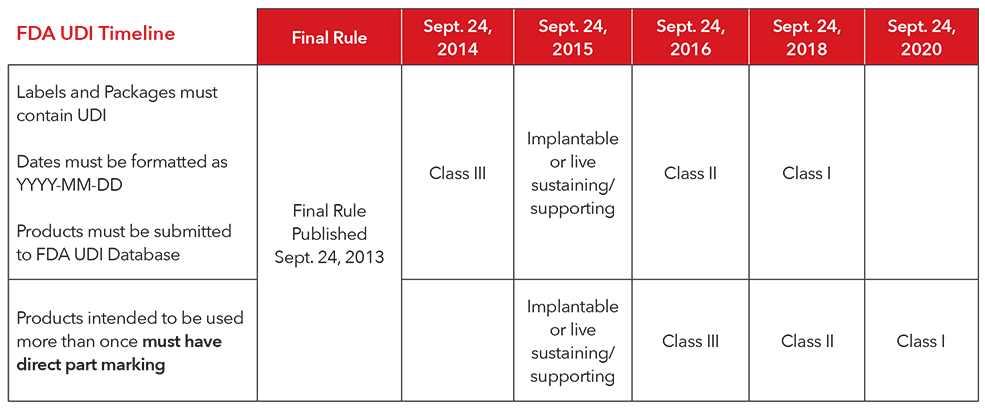
** Masimo führt freiwillig eine direkte Teilemarkierung bei allen wiederverwendbaren Produkten durch. Gemäß des aktuell gültigen Beschlusses der FDA ist es nicht erforderlich, dass Produkte von Masimo eine direkte Teilemarkierung erhalten.
4. Wie hält Masimo die UDI-Verordnung ein?
Masimo vertreibt Produkte der Klasse II und einige Produkte der Klasse I. Masimo hat die Kennzeichnung entsprechend den Anforderungen der UDI-Verordnung und GS1-Standards aktualisiert.
Bitte beachten Sie, dass alle Produkte, die NICHT als medizinisches Gerät klassifiziert sind, keinen Barcode tragen müssen.
5. Wie werden meine UDI-Kennzeichnung und meine direkte Teilemarkierung aussehen?
Unten befinden sich Beispiele für:
- Kennzeichnung der Sensorschachtel – bisherige Version und aktualisierte UDI-Kennzeichnungen
- Sensor mit direkter Teilemarkierung
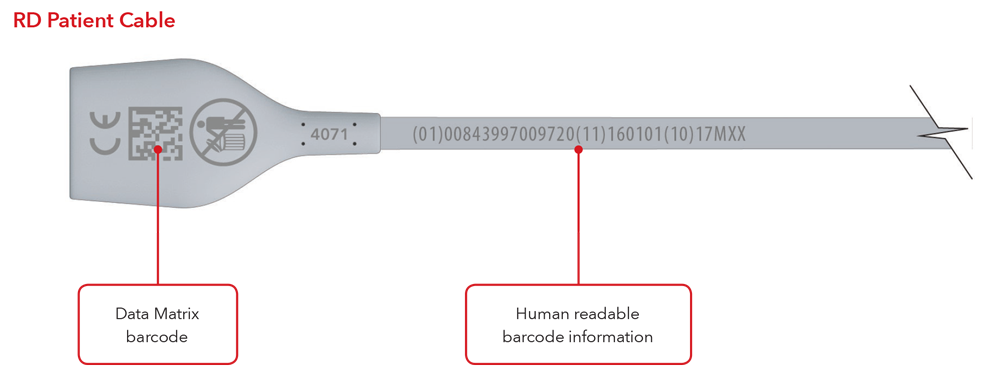
- Kabel mit direkter Teilemarkierung
Bitte beachten: Je nach Produkttyp wird die Kennzeichnung eine von zwei Datumsangaben enthalten. Produkte mit einem "Verwendbar bis"-Datum enthalten dies im Format JJJJ-MM-TT unter dem Verfallssymbol; zudem wird es innerhalb der GS1- und 2D-Barcodes nach dem vorangestellten Produktionscode (17) als JJMMTT codiert. Bei Produkten ohne „Verwendbar bis”-Datum wird das Herstelldatum im Format JJJJ-MM-TT neben dem Symbol für das Herstelldatum aufgeführt und innerhalb der GS1- und 2D-Barcodes nach dem vorangestellten Produktionsidentifikator (11) als JJMMTT codiert.
Beispiele für Kennzeichnungen der Sensorschachtel
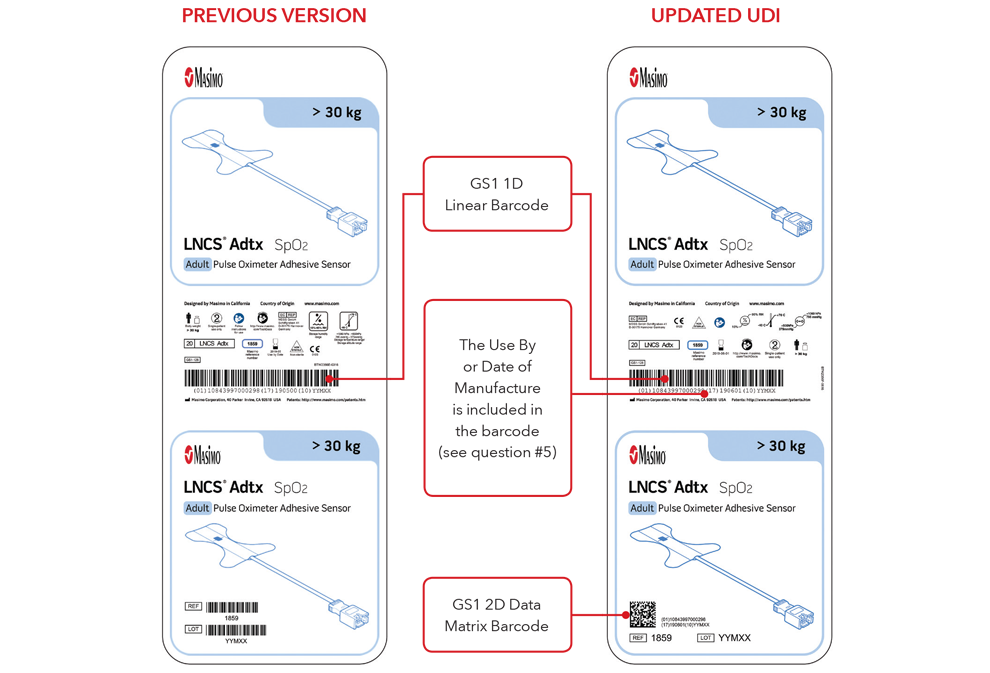
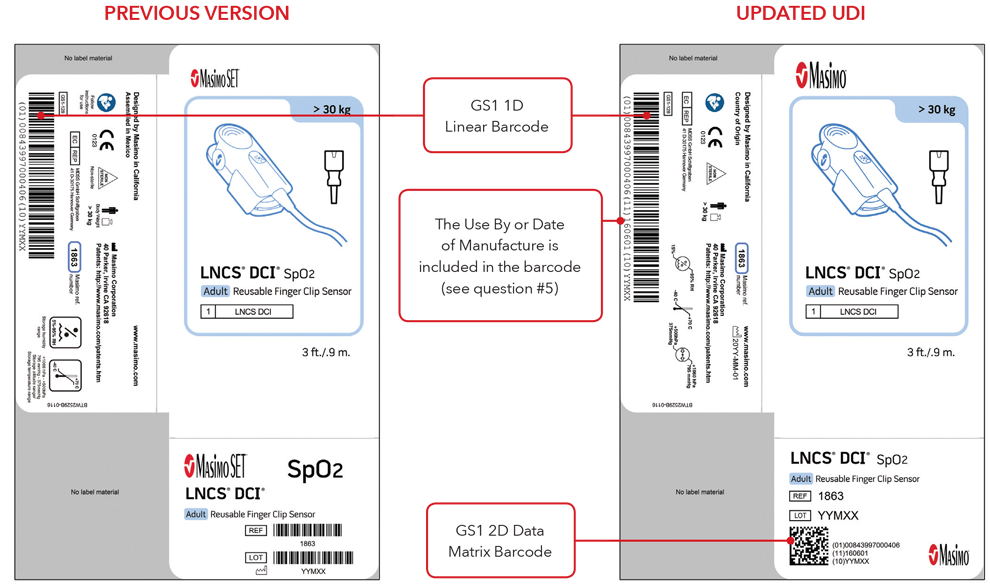
Beispiele für Sensor und Kabel mit direkter Teilemarkierung
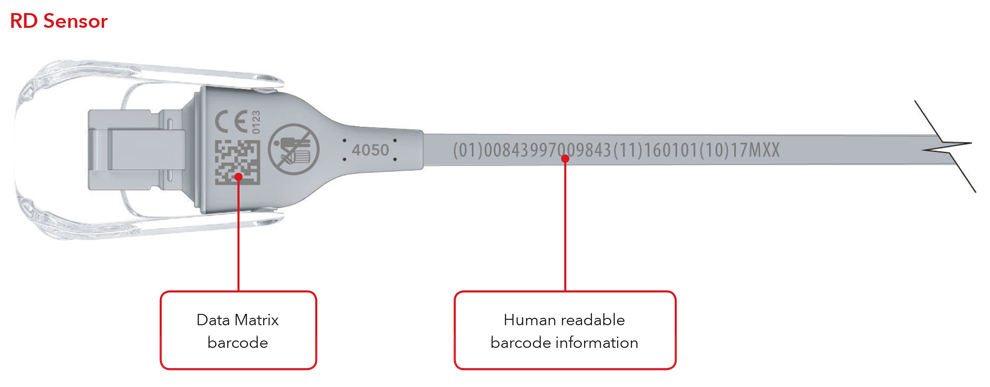
6. Was ist eine GTIN (Global Trade Item Number)?
Eine GTIN ist eine weltweit einzigartige GS1-Identifikationsnummer, mit der ein „Handelsobjekt” (Trade Item) identifiziert wird. GTINs werden vom Markeninhaber (der kennzeichnenden Stelle) des Produkts zugewiesen und dienen dazu, Produkte auf ihrem Weg durch die globale Lieferkette bis zum Endverbraucher, wie z. B. einem Krankenhaus, zu identifizieren. Wenn Sie gegenwärtig das GS1-System mit GTINs nicht für Ihr Produktmanagement verwenden, müssen Sie die GTINs für die Produkte, die Sie erwerben, beziehen.
Weitere Informationen über GTINs sind von GS1 erhältlich unter: https://www.gs1us.org/resources/standards.
7. Wie erhalte ich Produkt-GTINs?
Schicken Sie eine E-Mail an den Kundenservice von Masimo:
USA: customerorders@masimo.com
Außerhalb der USA: emeasales@masimo.com
Bitte geben Sie in der E-Mail Ihre Kundenkennung und die Teilenummer(n) des Produkts an.
8. Ich bin gegenwärtig für das Eingeben oder Scannen der CHARGEN- und/oder REF-Barcodes auf dem Etikett verantwortlich. Sollte ich hier mit Änderungen rechnen?
Ja. Die CHARGEN- bzw. REF-Barcodes auf dem Etikett werden entfernt und mit Text ersetzt, der nicht mehr gescannt werden kann. Für die CHARGEN-Information scannen Sie entweder den GS1-Barcode oder Sie finden sie neben dem CHARGEN-Symbol auf dem Etikett. Die REF-Information ist in der jeweiligen GTIN zu finden. Weitere Informationen über GTINs siehe Frage Nr. 6 oben.
9. Ändern sich mit der Einführung der UDI-Kennzeichnung die Produktnummern von Masimo?
Nein, die Produktnummern von Masimo bleiben die selben.
10. Was ist das neue, standardisierte Datumsformat und ab wann ist es gültig?
Der UDI-Beschluss hat das standardisierte Datumsformat "JJJJ-MM-TT" auf Gerätekennzeichnungen festgelegt. Spätestens ab dem Datum, ab dem eine Gerätekennzeichnung ein UDI enthalten muss, werden die Daten auf den Kennzeichnungen im neuen Format angegeben sein. Weitere Informationen über den Zeitrahmen für die Umsetzung, siehe Frage Nr. 3 oben.
11. Stellt Masimo Produktinformationen online zur Verfügung?
Die GUDID ist eine öffentlich zugängliche Datenbank, die für jedes medizinische Gerät den Teil der UDI mit der Gerätekennung (DI) und andere notwendige Produktinformationen enthält. Alle Unternehmen, die medizinische Geräte herstellen, müssen der GUDID die DI-Informationen zur Verfügung stellen. Masimo hat damit begonnen, Daten an die GUDID zu übermitteln und stellt sicher, dass alle Produkte rechtzeitig oder noch vor den festgelegten Zeitpunkten für die Einführung des UDI-Systems dort zu finden sind.
12. Was ist mit bereits auf Lager vorhandenen Produkten? Müssen sie von den Herstellern neu gekennzeichnet werden?
Nein, es gibt zwei Ausnahmen für bereits vorhandene Produkte:
- Geräte, die sich vor dem festgelegten Datum im kommerziellen Vertrieb befinden, müssen diesem endgültigen Beschluss nicht Folge leisten.
- Geräte, die vor dem festgelegten Datum hergestellt und gekennzeichnet worden sind, sind ebenfalls ausgenommen. Diese Ausnahme verfällt jedoch 3 Jahre nach dem festgelegten Gültigkeitsdatum.
13. Müssen alle Geräte eine direkte Markierung mit ihrer UDI erhalten?
Nein. Der Beschluss sieht lediglich die Markierung wiederverwendbarer medizinischer Geräte vor, die vor der Wiederverwendung eine intensive Reinigung/Sterilisation durchlaufen müssen.
Masimo führt freiwillig eine direkte Teilemarkierung bei allen wiederverwendbaren Produkten durch. Gemäß des aktuell gültigen Beschlusses der FDA ist es nicht erforderlich, dass Produkte von Masimo eine direkte Teilemarkierung erhalten. Weitere Informationen über den Zeitrahmen für die Umsetzung der direkten Teilemarkierung, siehe Frage Nr. 3 oben.
Weitere Informationen über das UDI-System finden Sie unter „Unique Device Identification (UDI)” auf der Webseite der FDA:
http://www.fda.gov/MedicalDevices/DeviceRegulationandGuidance/UniqueDeviceIdentification/
Wenn Sie weitere Fragen dazu haben, wie Masimo die UDI-Verordungen einhält, wenden Sie sich bitte an den Kundenservice von Masimo unter:
USA: customerorders@masimo.com
Außerhalb der USA: emeasales@masimo.com
PLCO-001927/PLMM-10045C-0818